放射治疗是肿瘤治疗中最常用的方法之一,但由于放射治疗的剂量限制和毒副作用,其疗效大打折扣。寻找低毒、高效的放疗增敏剂一直是临床上亟待解决的问题。在众多放疗增敏剂中,基于高原子序数(High-Z)的配位配合物,结构明确、性质可调,在X射线作用下通过光电效应和康普顿效应,提高放疗疗效,近年来备受关注。
近日,本课题组在基于配合物的放疗增敏剂设计上获得新突破,在国产权威期刊《Chin Chem Lett》(2021,32, 158-161)上发表了题为“Substituent-regulated highly X-ray sensitive Os(VI) nitrido complex for low-toxicity radiotherapy”的研究成果,该研究成果受到了杂志的专题报道和推广。暨南大学为该研究的唯一完成单位,暨南大学化学与材料学院硕士陈茗凯和黄小婷为文章的共同第一作者,暨南大学马丽副研究员和陈填烽教授为论文的通讯作者。

目前报道的配合物放疗增敏剂中,大部分为基于铂(Z=78)构建的配合物,此外,基于铱(Z=77)和钌(Z=44)构建的配合物也被报道为潜在的放疗增敏剂。与此同时,与铂Z值相近、Ru的同族元素Os(Z=76)构建的配合物却无人报道用于放疗增敏。在此,我们报道了第一个基于Os的配合物放疗增敏剂,OsN(PhenOH)Cl3 (PhenOH=1,10-菲咯啉-2-醇)。通过取代基调控,在配体上引入OH基团作为强给电子取代基的代表合成了OsN(PhenOH)Cl3,通过OH基团给电子效应,增大了OsN(PhenOH)Cl3中的Os-Cl和Os≡N的电子云密度,减小了Os-Cl和Os≡N的键长,进而降低了OsN(Phen)Cl3的毒性,设计合成了一种高效低毒的辐射增敏剂OsN(PhenOH)Cl3。通过进一步的研究发现,该放射增敏剂可以通过诱导细胞内ROS过量产生导致G2/M细胞周期阻滞进而杀伤肿瘤细胞。本研究为今后合理设计基于金属配合物的高效低毒放射增敏剂用于肿瘤的选择性治疗提供了依据。
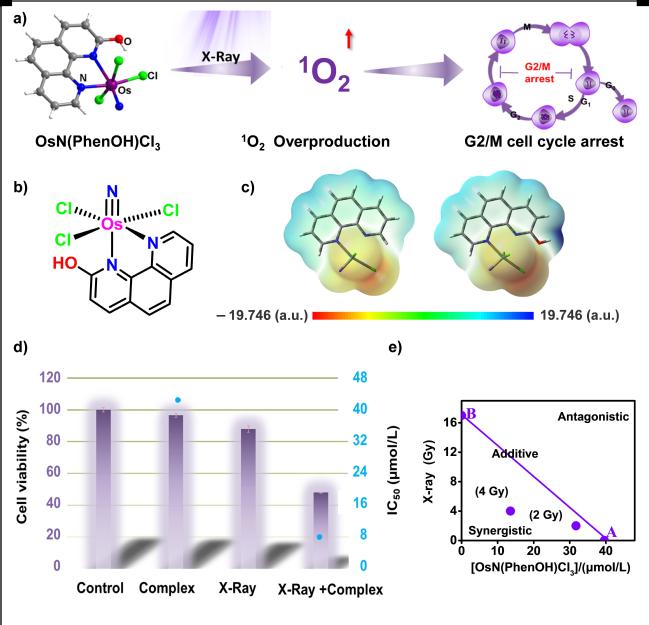
图1 (A)对X射线高度敏感的低毒放射治疗性Os(VI)氮配合物诱导G2/M细胞周期阻滞。(B) OsN(PhenOH)Cl3的结构。(C) OsN(Phen)Cl3和OsN(PhenOH)Cl3的MESP图。红色、灰色、蓝色、绿色和白色的原子分别表示氧、碳、氮、氯和氢。(D) OsN(PhenOH)Cl3 (2.5 mmol/L)加或不加X射线(4Gy)对Hela细胞的细胞毒作用。(E)X射线和OsN(PhenOH)Cl3联合处理对Hela细胞协同抑制增殖作用的等位相图分析。等谱图中的数据点对应于联合处理中50%的生长抑制率。
陈填烽教授团队一直致力于靶向化学创新药物的应用研究,获得万人计划青年拔尖人才项目、国家863计划、国家自然科学基金项目及广东省自然科学杰出青年基金等项目的资助。近五年以通讯作者在Cell子刊Matter、Science Advances、JACS、Angew Chem Int Ed等主流杂志发表论文超过250篇,其中IF>10有55篇,封面论文38篇,h-index 61,连续两年(2019、2020)入选“中国高被引学者”榜单。申报中国专利60项,实现技术成果转化12项。以第一完成人获得2021年高等学校科学研究优秀成果奖技术发明二等奖、2018年中华医学科技奖青年科技奖、2018广东省自然科学二等奖。
论文信息:Mingkai Chen#, Xiaoting Huang #, Jie Lai, Li. Ma*, Tianfeng Chen*. Chin Chem Lett, 2021,32, 158-161.
论文链接:https://www.sciencedirect.com/science/article/pii/S1001841720306914



