近期,温州医科大学附属第二医院朱雪琼教授团队与暨南大学化学与材料学院的陈填烽教授团队合作,在著名学术期刊Biomaterials(影响因子:15.304)上发表了题为“Therapeutic application of manganese-based nanosystems in cancer radiotherapy” 的论文,讨论了关于用于癌症放射治疗的锰基纳米系统及其进一步的临床应用。

癌症目前被列为全球人口最常见的死亡原因之一。放射治疗是癌症治疗的重要手段之一。放疗能够直接损伤DNA,从而抑制细胞增殖,甚至导致细胞坏死或凋亡。同时,放疗可通过产生活性氧等自由基间接破坏生物大分子物质的结构,并通过化学反应造成DNA结构损伤,从而导致细胞死亡。此外,活性氧还能通过激活相关蛋白通路来增加肿瘤细胞的凋亡以及引发脂质过氧化而诱导铁死亡。然而,肿瘤微环境弱酸性、缺氧和高谷胱甘肽等特点限制了放射治疗的疗效。另一方面,放疗也存在剂量相关毒性和损伤周围正常组织等临床问题。因此,提高抗辐射癌症的治疗效果并预防复发,同时最大限度地减少对健康组织的有害影响,成为了放射治疗临床应用中最需要攻克的难关。
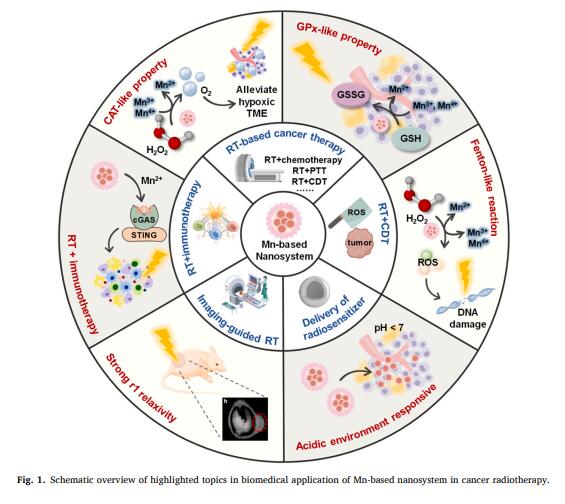
随着过去几年纳米生物技术的快速发展,研究人员开发并合成了越来越多的用于放射增敏治疗的纳米材料。锰是一种过渡金属元素,具有多种价态和存在形式。同时,锰基纳米材料由于其过氧化物酶和超氧化物歧化酶特性,对TME反应良好,缓解缺氧并降低高GSH。因此,锰基纳米材料因其独特的理化性质和优越的生物安全性,在过去二十年被广泛合成作为放射增敏剂。
该综述以锰基纳米材料在癌症放射治疗中的应用为切入点,着重介绍了锰基纳米粒子的特性与设计、用于癌症治疗的锰基放射增敏剂和用于影像引导放射治疗的锰基放射增敏剂。锰基纳米材料具有巨大的潜力,可以提高放疗的疗效并减少副作用。该综述为未来癌症治疗方法的发展提供了重要的启示,并为研究人员提供了进一步探索锰基纳米系统的方向。希望这一领域的研究能够取得更多的突破,为癌症患者提供更有效的治疗选择。相关工作得到了国家卫生健康委科学研究基金-浙江省医药卫生重大科技计划、浙江省中医药重点实验室项目的资助,博士研究生潘舒雅、博士研究生孙正伟为本论文共同第一作者,陈填烽教授和朱雪琼教授为通讯作者。
原文链接: https://www.sciencedirect.com/science/article/pii/S0142961223003290?via%3Dihub
课题组简介
温州医科大学朱雪琼教授团队主攻妇科肿瘤,尤其是良恶性子宫肌瘤的鉴别和宫颈癌的个体化治疗。为中国医促会妇产科专业委员会常务委员、浙江省医学会妇科肿瘤学分会副主任委员等,获得浙江省“万人计划”科技创新领军人才、省新世纪151人才第一层次、省卫生领军人才(培养对象)、省高校中青年学科带头人等。主持各级各类课题37项,包括国家自然科学基金项目6项、省部级课题8项。以第一作者或通讯作者发表论文287篇,其中SCI收录146篇,中华系列杂志30来篇。参编妇产科相关的著作或教材11部,其中主编4部、副主编1部。主持的成果获科技奖项12项,包括省科学技术奖3项,厅局级一等奖2项。授权专利18项,其中3项已经开发应用于临床宫颈癌的筛查和诊治中。
暨南大学陈填烽教授团队一直致力于以临床问题为导向的化学创新药物设计与诊疗应用研究,担任Journal of Nanobiotechnology副主编、Nano Research、Chinese Chemical Letters、Smart Materials in Medicine杂志编委。国家杰出青年基金获得者、万人计划、教育部新世纪优秀人才、国家863青年科学家、霍英东青年教师。研究方向为硒纳米医学与肿瘤精准放射和免疫治疗。针对肿瘤特殊理化性质,采用多级靶向策略,构筑含硒纳米药物,对肿瘤实施精准靶向增敏放疗,同时对肿瘤定向免疫增强,实现肿瘤的精准放免治疗。相关研究成果发表在Sci. Adv、Matter、JACS、Angew. Chem. Int. Ed.及ACS Nano等本领域主流期刊,授权国家发明专利35项,获高等学校科学研究优秀成果奖技术发明二等奖、中国抗癌协会科技二等奖、广东省自然科学二等奖、中华医学会青年科技奖等科技奖励。


