近日,本课题组陈填烽教授团队和哈佛医学院陶伟教授团队合作在口服凝胶微珠介导的原位合成硒蛋白用于调节肠道免疫和微生物群尤其是缓解炎症性肠病IBD方面取得了重要研究进展,相关研究成果 “Oral Hydrogel Microbeads-Mediated In Situ Synthesis of Selenoproteins for Regulating Intestinal Immunity and Microbiota”以封面论文形式发表于国际顶级期刊《Journal of the American Chemical Society》杂志(影响因子:16.383)。暨南大学陈填烽教授和哈佛医学院陶伟教授为该文章的共同通讯作者,课题组欧阳江博士和邓博硕士为本论文的共同第一作者。

硒蛋白在免疫细胞和炎症调节中起着至关重要的作用。然而,作为一种在胃酸性环境中易变性或降解的蛋白质类药物,硒蛋白的高效口服给药面临着巨大的挑战。在此,我们创新了一种基于口服水凝胶微珠的生化策略,可以原位合成硒蛋白,因此绕过了口服蛋白类药物递送存在的必要性和苛刻条件,同时有效地产生用于治疗应用的硒蛋白。水凝胶微珠是通过用海藻酸钙 (SA) 水凝胶保护壳包裹透明质酸修饰的硒纳米粒子合成的。
我们在患有炎症性肠病 (IBD) 的小鼠中测试了这一策略,IBD 是与肠道免疫和微生物群相关的最具代表性的疾病之一。我们的研究结果表明,水凝胶微珠介导的硒蛋白原位合成可以显著减少促炎细胞因子的分泌并介导免疫细胞(例如,减少中性粒细胞和单核细胞并增加免疫调节性 T 细胞),从而有效缓解结肠炎相关症状。该策略还能够调节肠道微生物群组成(增加益生菌丰度并抑制有害群落)以维持肠道稳态。考虑到与癌症、感染、炎症等广泛相关的肠道免疫和微生物群,这种原位硒蛋白合成策略也可能广泛应用于应对各种疾病。
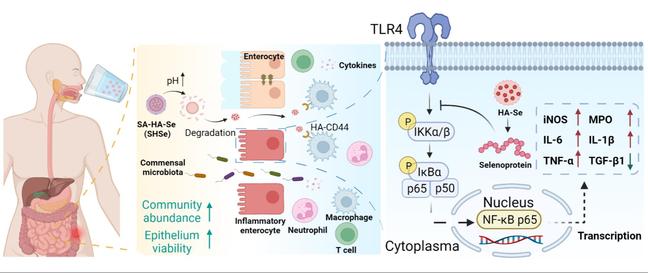
综上所述,该研究提出了一种基于新型口服核壳结构SHSe纳米硒凝胶微珠的原位合成硒蛋白的创新性口服递送策略。基于高效静电纺丝技术构建的含硒口服药物可在体内原位合成活性生物蛋白的构想,为口服蛋白类药物的设计提供了典型的参考范式,也为综合治疗胃肠道相关疾病等提供了新的见解。
陈填烽教授,暨南大学教授,国家杰出青年基金获得者、万人计划青年拔尖人才、国家863青年科学家、教育部新世纪优秀人才、霍英东青年教师奖获得者、广东省杰青/特支计划入选者。现任化学与材料学院副院长,附属第一医院纳米诊疗研究所所长,广东省纳米化学创新药物工程技术研究中心主任。研究方向为硒纳米医学与疾病精准诊疗应用。相关研究成果在Signal Transduct.Target. Ther.,Cell子刊Matter,Sci. Adv.,J. Am. Chem. Soc.,Angew. Chem. Int. Ed., Adv. Funct. Mater., Biomaterials等本领域IF>10期刊发表论文86篇,封面论文41篇,h-index73,连续三年入选“中国高被引学者”榜单;2021、2022年入选全球顶尖10万科学家榜单。申报中国专利92项,授权国家发明专利23项,实现技术成果转化13项,实现了纳米硒GMP吨级生产,并开展多中心临床研究。以第一完成人获得2020年高等学校科学研究优秀成果奖技术发明二等奖,2020年中国抗癌协会科技二等奖,2018年中华医学科技奖青年科技奖,2018广东省自然科学二等奖等科技奖励。
原文链接:https://doi.org/10.1021/jacs.3c02179